1.2 TEORIA ELETRÔNICA DA MATÉRIA
Sabe-se que toda matéria é formada de moléculas. Como exemplo, podemos citar a água, cuja molécula é H2O ou seja, dois átomos de hidrogênio e um átomo de oxigênio. Os átomos constituem a menor porção da matéria, que conserva as propriedades do elemento em seu estado normal. Cada átomo possui uma zona central e uma região que a circunda, sendo ambas denominadas de, respectivamente, núcleo e eletrosfera. No núcleo existem os prótons e os nêutrons e na eletrosfera situam-se os elétrons. Estas três partículas elementares são apenas algumas entre outras tantas que existem nos materiais.
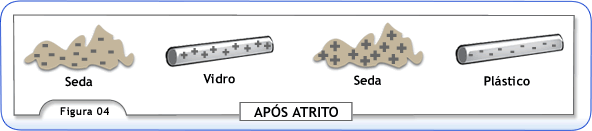
Ao elétron foi atribuída uma carga negativa devido a descoberta de que o bastão de plástico quando atritado com seda, nas experiências realizadas, ficava com predominância destas partículas. No caso do bastão de vidro atritado com a seda as partículas elementares que predominam nele são os prótons e, de acordo com a convenção feita, foi atribuída a estas partículas uma carga positiva .
ELÉTRON ---> CARGA ELÉTRICA NEGATIVA (-)
PRÓTRON ---> CARGA ELÉTRICA POSITIVA (+)
|
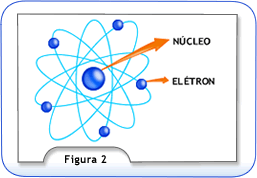
Na Figura 2, está representado um modelo atômico. O núcleo, devido a presença dos prótons, possui uma carga positiva, a qual é responsável pela força de atração que mantém os elétrons, girando nas suas respectivas trajetórias.
As minúsculas partículas que giram em torno do núcleo (elétrons) são submetidas a forças elétricas que variam de elétron para elétron, dependendo da posição destes.
| |
|
|
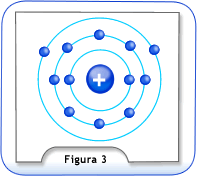
Na Figura 3, temos um átomo representado por várias camadas, além do núcleo. Em cada camada existem alguns elétrons, sendo a mais importante para o estudo das propriedades elétricas, a camada mais externa, chamada “camada de valência”. O núcleo é o responsável pela manutenção dos elétrons no átomo. Esta força de atração exercida pelo núcleo sobre os elétrons depende muito da distância, pois, quanto mais distante do núcleo estiverem os elétrons, menor será a força de atração e mais facilmente eles poderão deslocar-se para outro átomo.
| |
|
Os elétrons, fracamente ligados ao seu respectivo núcleo, que estão situados na última camada (camada de valência), isto é, na camada mais distante do núcleo, são chamados de “eletrons livres” . Assim, por exemplo, em 1g de cobre temos cerca de 1022 elétrons livres.
Como os prótons são partículas que, normalmente, estão fixas no núcleo e os elétrons podem se transferir de um átomo para outro, no nosso estudo vamos nos preocupar sempre com a “falta ou excesso de elétrons” , no átomo ou nos corpos.
Nos experimentos mencionados anteriormente, a seda, inicialmente, estava neutra , ou seja, o mesmo número de prótons e elétrons. Ao ser atritada com o plástico, este ficou com carga negativa, devido ao número de elétrons ser superior ao de prótons. Estes elétrons ganhos pelo plástico foram cedidos pela seda, na qual, existe agora um número de elétrons inferior ao de prótons. Logo, o número de elétrons sendo inferior ao de prótons, na seda, esta ficará carregada positivamente (deficiência de elétrons).
No caso do bastão de vidro, este carregou-se positivamente, logo cedeu elétrons para a seda, a qual ficou carregada negativamente (excesso de elétrons).
Conclui-se, conforme Figura 4, que um mesmo corpo pode carregar-se positivamente ou negativamente, dependendo da substância com a qual ele é atritado.